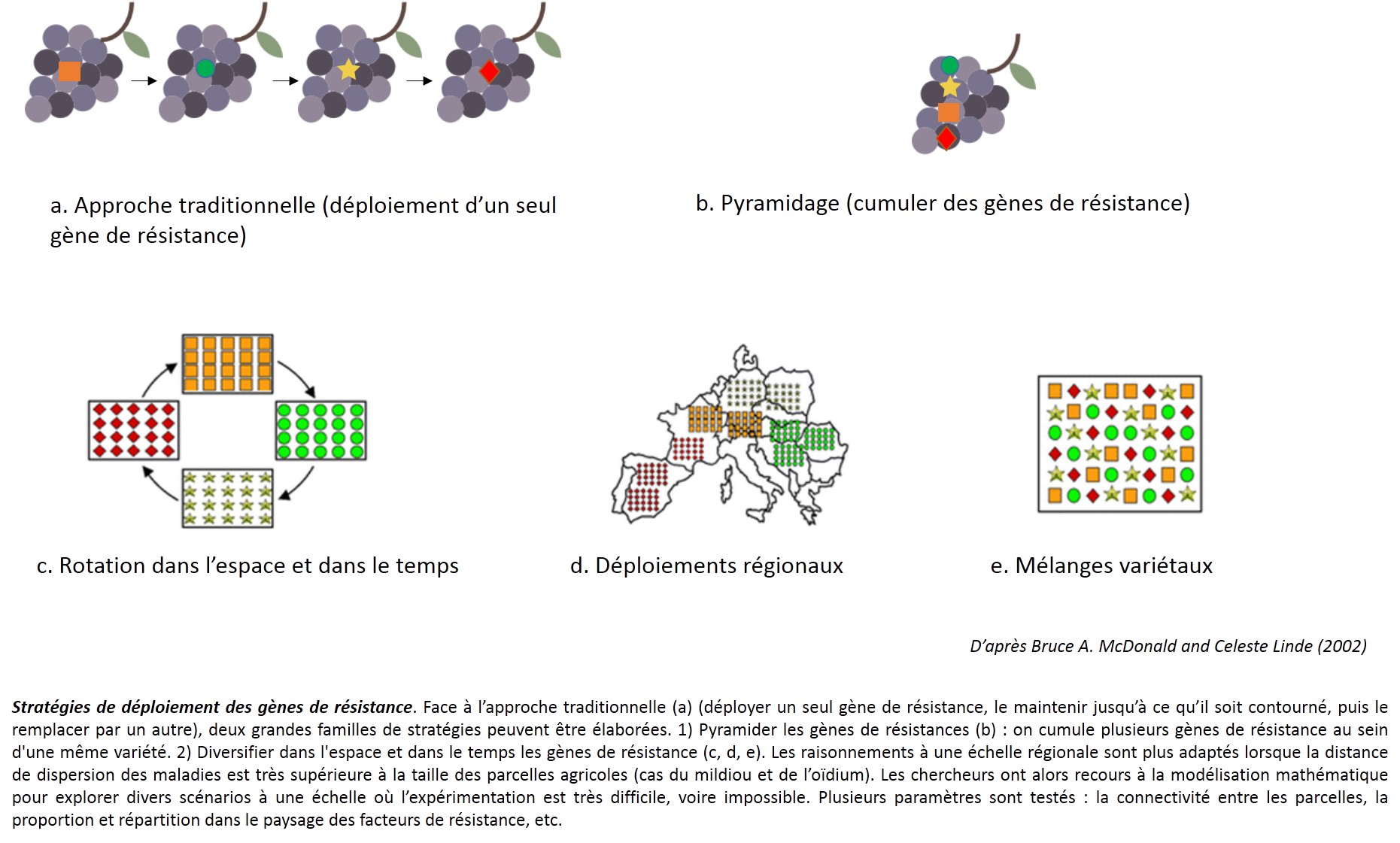
Les gènes de résistance ne sont pas éternels !
L’effet des gènes de résistance n’est pas éternel. Si certaines résistances restent efficaces de nombreuses années (citons la résistance au phylloxéra, introduite grâce à des portes greffes américains à la fin du XIXe siècle) d’autres perdent plus ou moins rapidement leur efficacité. Un exemple édifiant est le gène de résistance Rlm1 au phoma du colza, (causé par le champignon Leptosphaeria maculans) qui a été contourné en 3 ans seulement en France (Rouxel et al., 2003). Toutes plantes et maladies confondues, dans la moitié des cas avérés des pertes d’efficacité, elles ont lieu dans les six premières années (McDonald & Linde, 2002).
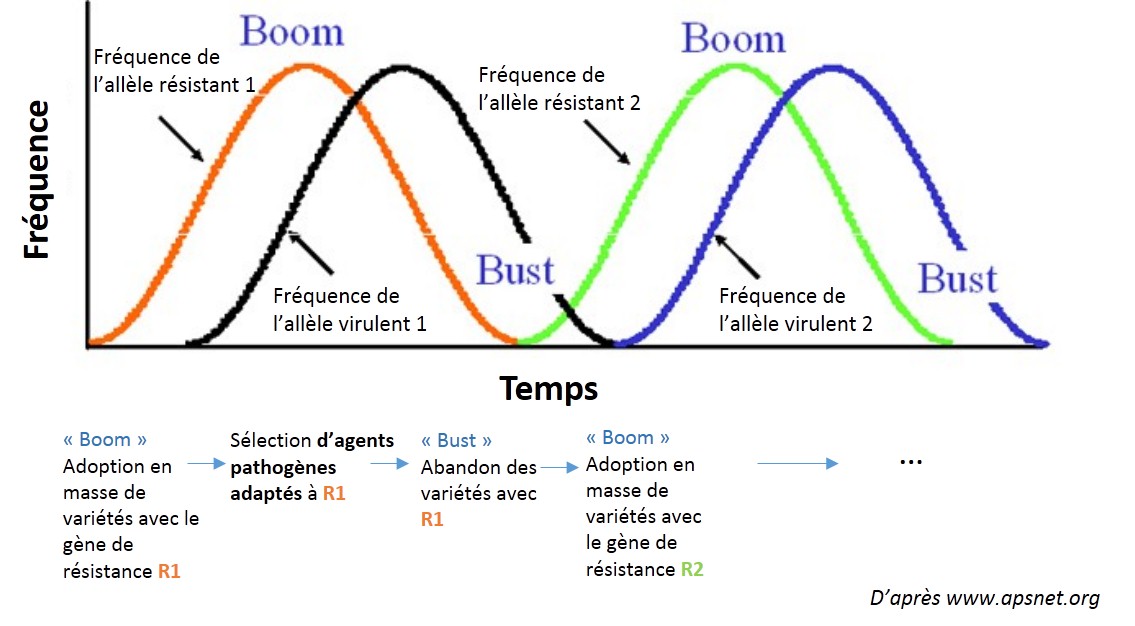 La raison de ces pertes d’efficacité ? Tout comme les bactéries s’adaptent aux antibiotiques, les bioagresseurs s’adaptent aux variétés résistantes, selon les mécanismes de la biologie évolutive¹. Ces adaptations entrainent une perte d’efficacité progressive des variétés résistantes. Au-delà d’un certain seuil de dégâts, les agronomes parlent de « contournement ». D’autres variétés avec un autre gène de résistance peuvent alors être introduites, qui seront eux-mêmes contournés et ainsi de suite, dans un cycle infernal du jeu du chat et de la souris… On parle de cycle de “Boom and Bust”, autrement dit « Emballement et abandon » (voir figure ci-contre).
La raison de ces pertes d’efficacité ? Tout comme les bactéries s’adaptent aux antibiotiques, les bioagresseurs s’adaptent aux variétés résistantes, selon les mécanismes de la biologie évolutive¹. Ces adaptations entrainent une perte d’efficacité progressive des variétés résistantes. Au-delà d’un certain seuil de dégâts, les agronomes parlent de « contournement ». D’autres variétés avec un autre gène de résistance peuvent alors être introduites, qui seront eux-mêmes contournés et ainsi de suite, dans un cycle infernal du jeu du chat et de la souris… On parle de cycle de “Boom and Bust”, autrement dit « Emballement et abandon » (voir figure ci-contre).
Ces contournements sont d’autant plus problématiques qu’il n’existe souvent qu’un petit nombre de résistances disponibles pour un bioagresseur donné (quand il en existe !). De fait, chaque contournement fragilise l’avenir du contrôle génétique des maladies et des ravageurs des plantes…
Résistance totale, résistance partielle ? On distingue deux grands types de résistance des plantes. Résistance totale : aussi nommée résistance qualitative, elle engendre une absence de maladie. Elle est généralement contrôlée par un gène majeur de résistance, correspondant à un gène d’avirulence de l’agent pathogène. Résistance partielle : aussi nommée résistance quantitative, elle conduit à une réduction de la maladie ciblée. Contrairement à la résistance totale, elle tend à être efficace contre toutes les souches d’une population pathogène.
En cas de perte d’efficacité de ces résistances, on parle de contournement pour une résistance qualitative -le gène n’est plus du tout efficace, il a été contourné -; et d’érosion pour une résistance quantitative (Niks et al., 2015). Exerçant une pression de sélection moindre sur le pathogène, les résistances partielles sont supposées plus durables. Associer dans une même variété résistance qualitative et quantitative assure une plus grande durabilité de la résistance (Brun et al., 2010).
Les facteurs de résistance de la vigne : un patrimoine fragile, à protéger
Chez la vigne (Vitis spp) ont été identifiés à ce jour 14 facteurs de résistance au mildiou (nommés Rpv), et
11 à l’oïdium (nommés Run ou Ren). Ils constituent un patrimoine fragile, leur efficacité, et donc leur utilité, étant soumises aux risques d’évolution des populations de pathogènes, d’autant plus que :
- L’oïdium et le mildiou de la vigne présentent un fort potentiel évolutif car ils combinent plusieurs caractéristiques favorisant leur adaptation (production d’une grande quantité de spores, bonnes capacités de dispersion, grande taille de population en Europe du fait des conditions climatiques favorables et de l’utilisation quasi exclusive de cépages sensibles…). Ce fort potentiel évolutif de l’oïdium et du mildiou de la vigne est illustré par la vitesse à laquelle ces deux agents pathogènes ont déjà répondu à la pression exercée par les fongicides en développant des résistances à presque toutes les molécules utilisées en quelques années seulement (Chen et al. 2007).
- Dans leur bassin d’origine (Amérique du Nord), l’oïdium et le mildiou sont tous deux capables d’infecter une large gamme d’espèces de Vitis spp, dont certaines sont parentes des cépages résistants récemment obtenus.
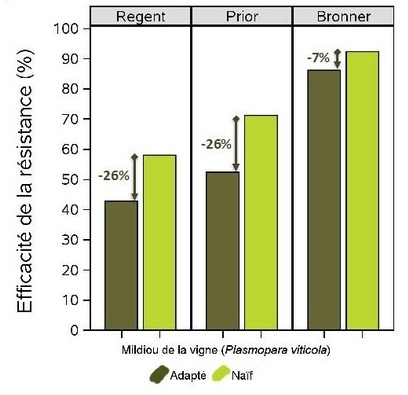
- Plusieurs cas avérés d’érosion de gènes de résistance ont été documentés pour le mildiou et l’oïdium : par exemple un premier cas a été décrit en 2010 sur la variété Bianca en Europe et des infections d’oïdium ont été observées sur des plantes porteuses d’un gène de résistance en Amérique du Nord. Deux études réalisées à l’INRA de Bordeaux ont de plus mis en évidence l’érosion de la résistance des variétés Regent, Prior et Bronner, déployées en Allemagne.
Dans un tel contexte, il est souhaitable de gérer de durablement les résistances introduites, ce qui passe par une combinaison de stratégies, qui permettent de réduire simultanément 1) le développement des épidémies à court terme et 2) la probabilité d’émergence de souches adaptées sur le long terme.
Quelles sont donc les stratégies mises en place pour les cépages résistants ?
- 1. Le pyramidage des gènes de résistance
L’association de plusieurs facteurs de résistance au sein d’une même variété, appelée pyramidage, est susceptible d’augmenter la durabilité de la résistance, en rendant le contournement plus difficile. C’est actuellement la stratégie du programme de création variétale (Resdur) de l’INRA lancé en 2000, et de la plupart des instituts de sélection européens actuellement.
- 2. Des systèmes de culture adaptés
 Avec le déploiement des cépages résistants en conditions de production, la question de leur intégration dans les systèmes de culture se pose. En effet, leur utilisation va modifier en profondeur non seulement les objectifs mais aussi les méthodes de protection. Ces systèmes de culture devront à la fois compléter l’efficacité partielle des gènes de résistance (notamment pour le mildiou), garantir leur durabilité, tout en maîtrisant les maladies et ravageurs non ciblés par le contrôle génétique.
Avec le déploiement des cépages résistants en conditions de production, la question de leur intégration dans les systèmes de culture se pose. En effet, leur utilisation va modifier en profondeur non seulement les objectifs mais aussi les méthodes de protection. Ces systèmes de culture devront à la fois compléter l’efficacité partielle des gènes de résistance (notamment pour le mildiou), garantir leur durabilité, tout en maîtrisant les maladies et ravageurs non ciblés par le contrôle génétique.
En pratique il s’agira de maîtriser les tailles de population des pathogènes visés par la résistance (mildiou, oïdium), ainsi que les autres pathogènes qui pourraient apparaître. Un essai mené par l’INRA de Bordeaux depuis 2011 a vu l’émergence de maladies secondaires habituellement maîtrisées par les fongicides. La plupart n’engendre que des dégâts mineurs (anthracnose, phylloxéra), mais d’autres mériteraient des stratégies de protection adaptées (pour le black-rot, le botrytis).
- 3. Un système de surveillance national : OSCAR !
La naissance d’OSCAR va permettre de sécuriser le déploiement des cépages résistants en France. Fort d’un réseau de suivi national, les objectifs de l’observatoire sont pluriels :
- Surveiller l’évolution des populations des agents pathogènes ciblés par les gènes de résistances grâce à la collecte régulière d’isolats de mildiou et d’oïdium sur le dispositif
- Détecter l’apparition de contournements, et l’apparition éventuelle de nouvelles problématiques sanitaires ;
- Identifier des systèmes de cultures adaptés
¹ Lorsque la méthode de contrôle est appliquée systématiquement et de façon soutenue dans le temps -par exemple le déploiement en masse de variétés avec un même gène de résistance – la forte sélection directionnelle qui en résulte se traduit par une adaptation rapide des agents pathogènes.
[faq cat_id= »34″]